《高考化學(xué)總復(fù)習(xí) 第十二章 物質(zhì)結(jié)構(gòu)與性質(zhì) 1231 考點一 晶體與晶胞基礎(chǔ)小題快練 新人教版》由會員分享���,可在線閱讀���,更多相關(guān)《高考化學(xué)總復(fù)習(xí) 第十二章 物質(zhì)結(jié)構(gòu)與性質(zhì) 1231 考點一 晶體與晶胞基礎(chǔ)小題快練 新人教版(5頁珍藏版)》請在裝配圖網(wǎng)上搜索����。
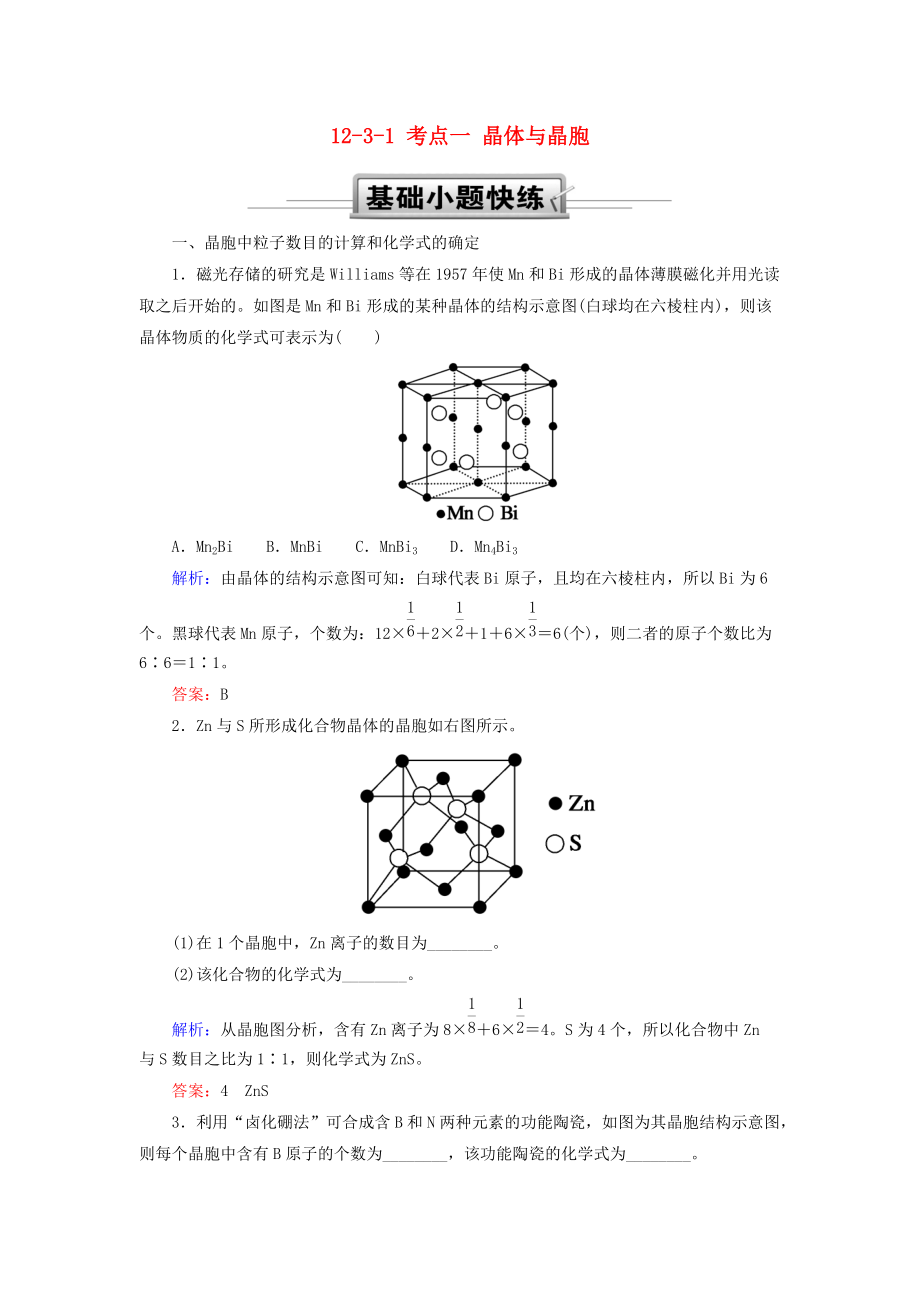
1�、12-3-1 考點一 晶體與晶胞一、晶胞中粒子數(shù)目的計算和化學(xué)式的確定1磁光存儲的研究是Williams等在1957年使Mn和Bi形成的晶體薄膜磁化并用光讀取之后開始的����。如圖是Mn和Bi形成的某種晶體的結(jié)構(gòu)示意圖(白球均在六棱柱內(nèi)),則該晶體物質(zhì)的化學(xué)式可表示為()AMn2BiBMnBiCMnBi3DMn4Bi3解析:由晶體的結(jié)構(gòu)示意圖可知:白球代表Bi原子���,且均在六棱柱內(nèi)�����,所以Bi為6個。黑球代表Mn原子��,個數(shù)為:122166(個)���,則二者的原子個數(shù)比為6611��。答案:B2Zn與S所形成化合物晶體的晶胞如右圖所示���。(1)在1個晶胞中�����,Zn離子的數(shù)目為_����。(2)該化合物的化學(xué)式為_���。解析:從晶
2��、胞圖分析����,含有Zn離子為864�。S為4個,所以化合物中Zn與S數(shù)目之比為11�����,則化學(xué)式為ZnS��。答案:4ZnS3利用“鹵化硼法”可合成含B和N兩種元素的功能陶瓷���,如圖為其晶胞結(jié)構(gòu)示意圖��,則每個晶胞中含有B原子的個數(shù)為_�,該功能陶瓷的化學(xué)式為_。解析:B的原子半徑比N大��,因而結(jié)構(gòu)示意圖中大球代表B原子�����,利用晶胞結(jié)構(gòu)可計算出每個晶胞中含有2個B和2個N����,化學(xué)式為BN。答案:2BN4如圖為甲����、乙���、丙三種晶體的晶胞:試寫出:(1)甲晶體化學(xué)式(X為陽離子)為_�。(2)乙晶體中A��、B��、C三種微粒的個數(shù)比是_�。(3)丙晶體中每個D周圍結(jié)合E的個數(shù)是_�����。解析:(1)甲中X位于立方體體心��,算作1�����,Y位于立方體
3���、頂點,實際占有:4�����,XY(個數(shù)比)21���,所以甲的化學(xué)式為X2Y���。(2)乙中A占有:81,B占有63��,C占有1�����,由此推出ABC(個數(shù)比)131。(3)丙中每個D周圍的E的個數(shù)與每個E周圍D的個數(shù)相同���,每個E周圍有8個D��,所以每個D周圍有8個E���。答案:(1)X2Y(2)131(3)8二、晶體的密度及微粒間距離的計算5O和Na能夠形成化合物F����,其晶胞結(jié)構(gòu)如圖所示,晶胞參數(shù)a0.566 nm��,F(xiàn)的化學(xué)式為_���;晶胞中O原子的配位數(shù)為_�;列式計算晶體F的密度(gcm3)_����。解析:O2半徑大于Na半徑�����,由F的晶胞結(jié)構(gòu)可知,大球代表O2�����,小球代表Na�,每個晶胞中含有O2個數(shù)為864,含有Na個數(shù)為8����,故O2、
4����、Na離子個數(shù)之比為4812,從而推知F的化學(xué)式為Na2O��。由晶胞結(jié)構(gòu)可知����,每個O原子周圍有8個Na原子,故O原子的配位數(shù)為8�����。晶胞參數(shù)a0.566 nm0.566107 cm,則晶胞的體積為(0.566107 cm)3����,從而可知晶體F的密度為2.27 gcm3。答案:Na2O82.27 gcm36某離子晶體晶胞的結(jié)構(gòu)如圖所示����,X()位于立方體頂點,Y()位于立方體中心�����。試分析:(1)晶體中距離最近的2個X與1個Y形成的夾角XYX是_�����。(2)設(shè)該晶體的摩爾質(zhì)量為M gmol1�,晶體的密度為 gcm3,阿伏加德羅常數(shù)的值為NA�����,則晶體中兩個距離最近的X之間的距離為_cm��。解析:(1)若將4個X連接
5��、�,構(gòu)成1個正四面體,Y位于正四面體的中心���,可聯(lián)系CH4的鍵角����,知XYX10928���。(2)摩爾質(zhì)量是指單位物質(zhì)的量的物質(zhì)的質(zhì)量�����,數(shù)值上等于該物質(zhì)的相對分子(或原子)質(zhì)量���。由題意知,該晶胞中含有個XY2或Y2X�����,設(shè)晶胞的邊長為a cm���,則有a3NAM�����,a�,則晶體中兩個距離最近的X之間的距離為 cm。答案:(1)10928(2) 7鑭鎳合金�、銅鈣合金及鈰鈷合金都具有相同類型的晶胞結(jié)構(gòu)XYn及很強的儲氫能力,其中銅鈣合金的晶胞結(jié)構(gòu)如圖所示����。試回答下列問題:(1)在元素周期表中Ca位于_區(qū)。(2)銅原子的基態(tài)原子核外電子排布式為_���。(3)已知鑭鎳合金LaNin晶胞體積為9.01023 cm3����,儲氫后形成
6�����、LaNinH4.5的合金(氫進入晶胞空隙���,體積不變)���,則LaNin中�,n_(填數(shù)值)�����;氫在合金中的密度為_�����。解析:(3)由銅鈣合金的晶胞結(jié)構(gòu)圖知���,銅、鈣合金中�,N(Cu)126615,N(Ca)1223����,因鑭鎳合金與銅鈣合金的晶胞結(jié)構(gòu)相同,則在LaNin中���,n5���。1 mol合金中含有NA個該合金的晶胞���,則9.01023 cm3NAM,0.083 gcm3��。答案:(1)s(2)1s22s22p63s23p63d104s1或Ar3d104s1(3)50.083 gcm38立方氮化硼和金剛石是等電子體�,其晶胞結(jié)構(gòu)如圖所示,則處于晶胞頂點上的原子的配位數(shù)為_����,若晶胞邊長為361.5 pm,則立方氮化硼
7���、的密度是_gcm3(只要求列算式���,不必計算出數(shù)值,阿伏加德羅常數(shù)的值為NA)��。解析:一個立方氮化硼晶胞中含有4個N原子和4個B原子�。一個晶胞的質(zhì)量為4 g,一個立方氮化硼晶胞的體積是(361.5 pm)3��,因此立方氮化硼的密度是 gcm3��。答案:49(1)用晶體的X射線衍射法可以測得阿伏加德羅常數(shù)�。對金屬銅的測定得到以下結(jié)果:晶胞為面心立方最密堆積�,邊長為361 pm��。又知銅的密度為9.00 gcm3��,則銅晶胞的體積是_cm3����、晶胞的質(zhì)量是_g�����,阿伏加德羅常數(shù)為_列式計算�����,已知Ar(Cu)63.6�。(2)CaO與NaCl的晶胞同為面心立方結(jié)構(gòu),已知CaO晶體密度為a gcm3��,NA表示阿伏加德
8�、羅常數(shù),則CaO晶胞體積為_cm3���。解析:(1)體積是a3���;質(zhì)量體積密度����;一個體心晶胞含4個原子�,則摩爾質(zhì)量四分之一晶胞質(zhì)量NA,可求NA��。(2)因為CaO與NaCl的晶胞同為面心立方結(jié)構(gòu)�。所以一個晶胞中有四個鈣離子和四個氧離子,根據(jù)M(CaO)56 gmol1�����,則一個CaO的質(zhì)量m(CaO) g��。V(CaO晶胞)質(zhì)量/密度 cm3����。答案:(1)4.7010234.231022NA6.011023 mol1(2)6EDBC3191F2351DD815FF33D4435F3756EDBC3191F2351DD815FF33D4435F3756EDBC3191F2351DD815FF33D4435F3756EDBC3191F2351DD815FF33D4435F3756EDBC3191F2351DD815FF33D4435F3756EDBC3191F2351DD815FF33D4435F375
 高考化學(xué)總復(fù)習(xí) 第十二章 物質(zhì)結(jié)構(gòu)與性質(zhì) 1231 考點一 晶體與晶胞基礎(chǔ)小題快練 新人教版
高考化學(xué)總復(fù)習(xí) 第十二章 物質(zhì)結(jié)構(gòu)與性質(zhì) 1231 考點一 晶體與晶胞基礎(chǔ)小題快練 新人教版